Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo Raffaele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1© i Concetta Lotti 2,*
- 1 Odsjek za nauku o tlu, biljkama i hrani, Jedinica za genetiku i oplemenjivanje biljaka Univerzitet u Bariju, Via Amendola 165/A, 70125 Bari, Italija; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (ARM); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Odsjek za poljoprivredu, hranu i okoliš, Univerzitet u Foggia, Via Napoli 25, 71122 Foggia, Italija
- 3 Odsjek za bionauke, biotehnologiju i biofarmaceutiku, Univerzitet u Bariju, Via Orabona 4, 70125 Bari, Italija; guglielmo.rainaldi@uniba.it
- 4 Odjel za energetske tehnologije, bioenergiju, biorafineriju i zelenu hemiju, ENEA Trisaia istraživački centar, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italija; paolo.iovieno@enea.it
* Korespondencija: rosa.mazzeo@unifg.it (RM); concetta.lotti@unifg.it (CL)
Sažetak:
luk (Allium cepa L.) je druga po važnosti povrtarska kultura u svijetu i nadaleko je cijenjena zbog svojih zdravstvenih prednosti. Uprkos značajnom ekonomskom značaju i njegovoj vrijednosti kao funkcionalne hrane, luk je slabo istražen u pogledu njegove genetske raznolikosti. Ovdje smo ispitali genetsku varijaciju “Acquaviva crvenog luka” (ARO), domaće sorte sa stoljetnom istorijom uzgoja u malom gradu u pokrajini Bari (Apulija, južna Italija). Skup od 11 mikrosatelitskih markera korišten je za istraživanje genetske varijacije u kolekciji germplazme koja se sastoji od 13 ARO populacija i tri uobičajena komercijalna tipa. Analiza genetičke strukture parametarskim i neparametarskim metodama istakla je da ARO predstavlja dobro definiran genski fond, koji se jasno razlikuje od rasa Tropea i Montoro s kojima se često griješi. Da bi se pružio opis lukovica koje se obično koriste za svježu potrošnju, ocijenjen je sadržaj rastvorljivih čvrstih supstanci i ljutina, pokazujući veću slatkoću u ARO u odnosu na dvije gore navedene domaće sorte. Sve u svemu, ova studija je korisna za buduću valorizaciju ARO-a, koja bi se mogla promovirati kroz oznake kvaliteta koje bi mogle doprinijeti ograničavanju komercijalnih prijevara i poboljšanju prihoda malih posjednika.
Uvod
Rod Allium obuhvata oko 750 vrsta [1], među kojima je crni luk (Allium cepa L., 2n = 2x =16) jedna od najrasprostranjenijih. A. cepa ima dvogodišnji ciklus i reproduktivno ponašanje izvan ukrštanja. Danas ga globalna proizvodnja luka (97.9 Mt) čini drugom najvažnijom povrtarskom kulturom nakon paradajza [2]. Od davnina se lukovica luka koristila i kao hrana i u narodnoj medicini. Zaista, stari Egipćani su već prijavili nekoliko terapeutskih formula zasnovanih na upotrebi belog i luka u medicinskom papirusu iz 1550. godine pre nove ere, Codex Ebers [3].
Ovo svestrano i zdravo povrće se konzumira sirovo, svježe ili kao prerađeni proizvod, a koristi se za poboljšanje okusa mnogih jela. Nekoliko novijih studija tvrdi da konzumacija luka može smanjiti rizik od kardiovaskularnih bolesti [4,5], gojaznosti [6], dijabetesa [7] i različitih oblika raka [8–10]. Zdravstvena svojstva luka se često pripisuju visokim nivoima dvije klase nutraceutskih jedinjenja: flavonoida i alk(en)il cistein sulfoksida (ACSO). Prva klasa uključuje flavonole i antocijanine. Kvercetin je glavni flavonol koji se može otkriti, poznat po svojim jakim antioksidativnim i protuupalnim svojstvima u uklanjanju slobodnih radikala i vezivanju jona prijelaznih metala [11]; dok antocijani daju crvenu/ljubičastu boju nekim sortama luka. Što se tiče ACSOs, najzastupljeniji je izoaliin [(+)-trans-S-1-propenil-L-cistein sulfoksid] [12], nehlapljiva i neproteinogena sumporna aminokiselina pohranjena u ćelijama, koja je indirektno odgovorna za oštru aromu i ukus luka [13]. Nakon oštećenja tkiva, izoaliin se cijepa od strane enzima aliinaze kako bi se proizveo niz hlapljivih spojeva (piruvat, amonijak, tiosulfonati i propantialni S-oksid) koji izazivaju suzenje i uzrokuju neprijatan miris (oporost) [14]. Oporost luka se često mjeri kao količina, po gramu svježe težine, pirogrožđane kiseline stvorene hidrolizom [15,16].
U zemljama mediteranskog basena, predložen kao jedan od sekundarnih centara raznolikosti A. cepa [17,18], lukovice luka pokazuju široku varijabilnost u obliku, veličini, boji, suhoj tvari i oštrini [19-jedan]. Štaviše, gnojidba na bazi sumpora, agronomske prakse, vrsta tla, klimatski uslovi i genotip sorti ili domaćih sorti mogu utjecati na kvalitet lukovice dajući posebne organoleptičke i nutritivne vrijednosti [23-jedan]. U Italiji, uprkos širokoj dostupnosti germplazme luka, samo nekoliko sorti luka često je podvrgnuto naučnim studijama i pravilno okarakterisano [28,29].
Temeljna genetska i fenotipska karakterizacija agrobiodiverziteta ključna je za osiguravanje odgovarajućeg očuvanja biljnih genetičkih resursa i promoviranje upotrebe specifičnih genotipova u lancu vrijednosti [30-jedan]. Markeri ponavljanja jednostavne sekvence (SSR) često su birani za mapiranje [33-jedan], DNK otisci prstiju i diskriminacija sorti [36-jedan]i pouzdanu procjenu genetičke varijabilnosti unutar i među rasama [39-jedan], budući da su specifični za lokus, multialelni, kodominantno naslijeđeni, visoko reproduktivni i pogodni za automatiziranu genotipizaciju.
U ovoj studiji svoju smo pažnju usmjerili na apulijsku tradicionalnu sortu, „crveni luk Acquaviva“ (ARO), koji se uzgaja prema metodama organske poljoprivrede u malom području grada Acquaviva delle Fonti, u pokrajini Bari. (Apulija, južna Italija). Lukovice ove sorte su velike i spljoštene i crvene boje i uglavnom se koriste u lokalnim receptima. Iako je ARO dobio oznaku kvalitete “Slow Food Presidium”, njegova bi proizvodnja mogla biti dodatno promovirana i zaštićena oznakama kvalitete Evropske unije kao što su zaštićena geografska oznaka (PGI) i zaštićena oznaka porijekla (POD), jer bi oni mogli doprinijeti ograničavanju komercijalne prijevare i poboljšati prihod malih posjednika. Ovdje su SSR molekularni markeri korišteni kao moćni alati za procjenu genetske varijacije među populacijama ARO i za razlikovanje ove domaće rase od druge dvije južnotalijanske domaće vrste crvenog luka. Nadalje, procijenili smo oporost i sadržaj rastvorljive čvrste supstance kako bismo procenili ukus ARO u odnosu na potražnju na tržištu.
Rezultati
Uspostavljanje Acquaviva kolekcije germplazme crvenog luka i morfološka karakterizacija
Sjeme 13 populacija ARO landrasa, koje su donirali farmeri u okviru projekta BiodiverSO Apulija Region, korišteno je za uspostavljanje kolekcije germplazme ARO.
Morfološki deskriptori, koji se odnose na lukovicu, kožicu i meso, prikupljeni su na ARO germplazmi i na tri vrste luka, dva pripadaju rodnoj rasi “Tropea crveni luk” (TRO) i jedan rodu “Montoro bakreni luk” (MCO) (slika 1). Sve ARO sijalice bile su ravne i karakterizirane su crvenom vanjskom kožicom i mesom s različitim nijansama crvene boje. Nasuprot tome, meso TRO sijalica bilo je potpuno crveno, dok je meso MCO sijalica bilo slabo pigmentirano (Tabela S1). Biohemijska analiza je omogućila da se proceni sadržaj čvrstih rastvora i oštrina. Kako je navedeno u tabeli 1, srednje vrijednosti čvrstog rastvorljivog sadržaja lukovica u populacijama ARO bile su 7.60, a kretale su se od 6.00 (ARO12) do 9.50° Brix (ARO11 i ARO13). Ova vrijednost je bila viša od one procijenjene za TRO i MCO landrase (4.25 i 6.00° Brix, respektivno).

Tabela 1. Vrijednosti čvrstog rastvorljivog sadržaja i oštrine procijenjene u populacijama “Acquaviva Red Onion” (ARO), “Tropea Red Onion” (TRO) i “Montoro Copper Onion” (MCO) *.
| ŠIFRA | Rastvorljivi čvrsti sadržaj (Brix) | oporost (pmolg-1 FW) | ||
| Srednje | CV y (%) | Srednje | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 na | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 na | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 na | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 na | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 na | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | 9.50 A | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | 9.50 A | 7.44 | 6.63 na | 24.93 |
| MKO | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
* Sredstva sa istim slovima u velikim ili malim slovima nisu statistički različita na 0.01P odnosno 0.05P (SNK-ov test). y Koeficijent varijacije.
Srednja vrijednost oštrine ARO, procijenjena sadržajem pirogrožđane kiseline, bila je 6.00, kretala se od 4.51 pmol g-1 FW (ARO6) do 7.04 (ARO8). Ova vrijednost je bila viša od one procijenjene u TRO i MCO landrasama (3.54 pmol g-1 FW i 4.18 pmol g-1 FW, respektivno).
SSR polimorfizam i genetski odnosi među akcesijama
U ovoj studiji, 11 od 37 testiranih kombinacija SSR prajmera dalo je polimorfizam sa jednim lokusom, tj. dajući najviše dva proizvoda amplifikacije u jednoj jedinki. Ukupno je otkriveno 55 alela kod 320 osoba s brojem alela po lokusu od 2 (ACM147 i ACM 504) do 11 (ACM132) i srednjom vrijednošću od 5 alela (Tabela 2). U pojedinačnim populacijama broj alela (Na) kretao se od 1.94 (ACM147 i ACM504) do 5.38 (ACM132), dok se efektivni broj alela (Ne) kretao od 1.41 (ACM152) do 2.82 (ACM449). Odstupanja između Na i Ne vrijednosti su posljedica prisustva alela sa niskom frekvencijom u populacijama i dominacije samo nekoliko alela. Najviša uočena vrijednost heterozigotnosti (Ho) istaknuta je za ACM138 i ACM449 (0.62), dok je najniža bila povezana sa ACM152 (0.25). Očekivana heterozigotnost (He), koja odgovara teorijskom očekivanju u panmiktičkoj populaciji, kretala se od 0.37 (ACM504) do 0.61 (ACM132, ACM138 i ACM449). Wrightov indeks fiksacije (Fis) je pokazao vrijednosti blizu nule (prosjek 0.05) za sve markere, što ukazuje na slične vrijednosti između uočenog i očekivanog nivoa heterozigotnosti, kao što se očekivalo za vrstu ukrštanja. Efikasnost pojedinačnog SSR markera u genetskom otisku prsta procenjena je indeksom polimorfnog sadržaja informacija (PIC), sa srednjom vrednošću od 0.48 i kretala se od 0.33 (ACM504) do 0.67 (ACM132). Drugi indeks efikasnosti, Šenonov indeks informacija (I) je pokazao srednju vrednost od 0.84, a pretpostavljene vrednosti su se kretale od 0.45 (ACM152) do 1.20 (ACM132).
Tabela 2. Karakteristike polimorfizma 11 SSR markera koji se koriste za procjenu genetičke raznolikosti u populacijama ARO, TRO i MCO. Ukupan broj alela (Na), raspon veličine pojasa i indeks polimorfnog sadržaja informacija (PIC) Pogledajte ukupan skup od 320 jedinki genotipiziranih u ovoj studiji. Broj alela (Na), broj efektivnih alela (Ne), uočena heterozigotnost (Ho), očekivana heterozigotnost (He), indeks fiksacije (Fis), a Šenonov indeks informacija (I) odnose se na srednje vrijednosti izračunate iz 16 populacija, od kojih je svaka sastavljena od 20 pojedinaca.
| Locus. | Total Na | Raspon veličina (bp) | PIC | Srednje | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Srednje | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Među populacijama, ARO3, ARO6, ARO8, ARO10, TRO1 i MCO su pokazali visok nivo genetske varijacije (Ho > 0.5), dok je najmanji diverzitet uočen u populaciji ARO7 (Ho = 0.27) (Dopunska tabela S2). Sve u svemu, svi aksesoari su pokazali Fis vrijednosti bliske nuli (Fis srednja vrijednost = 0.054), kao što se očekivalo pod nasumičnim uvjetima parenja.
Analiza molekularne varijanse i genetičke strukture
AMOVA je izračunala hijerarhijsko podjelu genetičke varijacije među i unutar populacija. Rezultati su istakli značajan dio genetske varijacije unutar populacija (87%). Varijacija među populacijama, 13%, bila je veoma značajna (P < 0.001) (Tablica 3). Parne vrijednosti parametra Fpt, analognog Wright-ovom Fst indeksu fiksacije, u rasponu od 0.002 (ARO2/ARO10) do 0.468 (ARO7/TRO2), bile su značajne (P < 0.05), osim za devet poređenja u paru (dodatna tabela S3).
Tabela 3. Analiza molekularne varijanse 320 genotipova iz 16 populacija allium cepa L.
| izvor | df | Zbir kvadrata | Procjena varijance | Varijanca (%) | Fpt | P |
| Među populacijama | 15 | 458.63 | 1.16 | 13% | ||
| Unutar populacija | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| ukupan | 319 | 2731.62 | 8.66 |
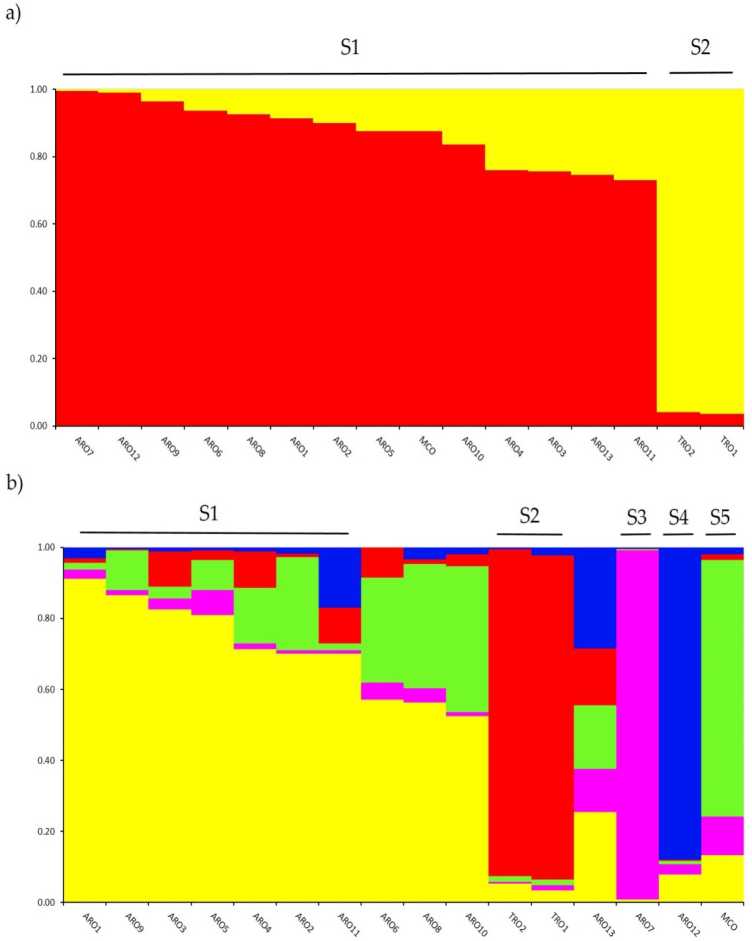
Istraživanje genetske strukture u A. cepa kolekcija genotipizirana u ovoj studiji obavljena je pomoću klasterske analize zasnovane na modelu primjesa implementirane u softverskoj STRUKTURI. Metoda Evanno AK predložila je podjelu u dva klastera (K = 2) kao najinformativniju za naše podataka,s the sljedeći najviši peak kod K = 5 (sopplementaiv Rgure S1). A viljuška = 2, ahpopulations were assigned takođernif dva klastera sa a rnernbertoip koeficijent (q) > 0.7. Kako shown in figura 2a, prvi klaster (nazvan S1) uključivao je MCO i sve ARO populacije, dok je S2 klaster grupisao dvije TRO populacije. Kod K = 5, pružajući dublji opis skupa podataka (Slika 2b), 75% pristupa je dodijeljeno jednom od pet klastera. Potvrđeno je razdvajanje između ARO (S1) i TRO (S2), iako su neke ARO populacije pomiješane (q < 0.7) ili grupisane odvojeno u dva nova klastera S3 i S4 (ARO7 i ARO12, respektivno). Zanimljivo je da je komercijalni tip MCO formirao poseban klaster (S5) odvojen od apulijskog crvenog luka.
Genetski odnosi među populacijama
SSR polimorfizam je omogućio da se nacrta dendrogram genetske raznolikosti, a rezultati filogenetske analize prikazani su na slici 3a. Ovdje je kolekcija germplazme podijeljena u pet grupa snažno podržanih početnim vrijednostima. Populacije ARO7 i ARO12 su odmah odvojene od preostalih populacija i formirale su dva različita klastera. Treći klaster je uključivao dvije komercijalne populacije TRO, dok je četvrti čvor dijelio MCO od jedanaest ARO populacija. Genetski odnos koji se javlja među populacijama dalje je istražen pomoću analize glavnih koordinata (PCoA) (Slika 3b). Kao što je ranije naglašeno, populacije ARO su bile grupisane usko, osim ARO12 i ARO7, koji su se pojavili na izolovanim pozicijama na PCoA dijagramu. Dvije TROs i MCO populacije bile su raštrkane u donjem desnom panelu grafikona.
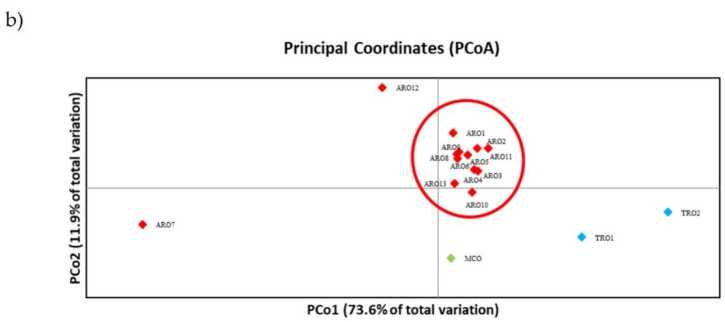
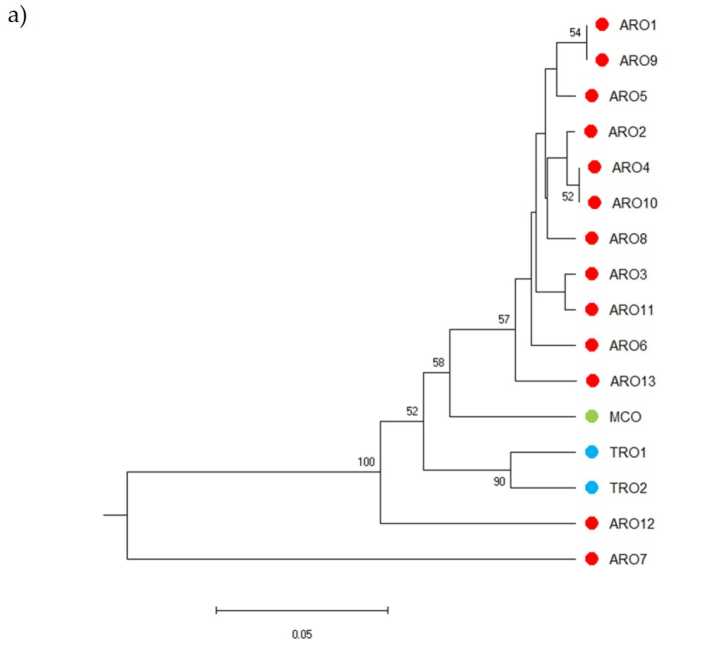
Slika 3. Genetska raznolikost među 16 A. cepa populacije okarakterisane u ovoj studiji, na osnovu njihovog SSR profila. (a) UPGMA dendrogram genetske udaljenosti. Vrijednosti podrške za Bootstrap >50 su naznačene iznad odgovarajućih čvorova; (b) analiza glavnih komponenti (PCoA). Klaster zaokružen crvenom bojom se u potpunosti poklapa sa grupom generiranom filogenetskom analizom i koju čini 11 ARO akcesija.
rasprava
U okviru velike količine agrobiodiverziteta koji se tradicionalno uzgaja u južnoj Italiji, sorte luka predstavljaju nišne proizvode koje je potrebno sačuvati od rizika genetske erozije i prijetnje zamjene modernim sortama. U okviru regionalnog projekta BiodiverSO, čiji je cilj prikupljanje, karakterizacija, promoviranje i očuvanje genetskih resursa regije Apulia koji su snažno povezani s lokalnim naslijeđem, uspostavili smo kolekciju sjemena od 13 populacija ARO landrace. Izvijestili smo o prvoj procjeni varijacije ARO u smislu polimorfizma DNK i dva biohemijska parametra, sadržaja rastvorljive čvrste materije i pirogrožđane kiseline, koji se odnose na svojstva ukusa i koji su od značaja za prihvatanje svježih nekuhanih proizvoda. Osim toga, podaci o rodnoj sorti ARO upoređivani su s onima prikupljenim na dvije druge vrste pigmentiranog luka s kojima se često griješi.
Biohemijske analize su istakle slatkoću 13 populacija ARO, povezanu sa visokim sadržajem rastvorljivih čvrstih supstanci i srednjom oštrinom, u skladu sa smernicama industrije slatkog luka [31]. ARO sijalice su bile slađe od onih kod TRO i MCO landrasa, i pokazale su nešto veću pikantnost. Međutim, slatkoća u luku je posljedica ravnoteže između sadržaja šećera i ljutine, stoga bi ova karakterizacija mogla biti korisna za podršku odabiru vrijednih genotipova, koji poljoprivrednici obično sprovode samo na osnovu morfologije.
Potvrđeno je da su SSR markeri korisno sredstvo za razlikovanje genotipova, iako prikupljeni u uskom rastućem području kao što je grad Acquaviva delle Fonti. Odabrani markeri su pokazali veći broj alela od markera koje su prethodno prijavili [43] i [44], ali niže od markera koje je prijavio [45]. Štaviše, 50% našeg seta markera pokazalo je vrijednosti PIC indeksa veće od 0.5, što se pokazalo prikladnim za diskriminaciju populacija u kolekciji, kao što sugerira [46]. Procjena raznolikosti unutar populacija otkrila je slične vrijednosti između Ho i He, što je rezultiralo niskim Fis vrijednosti. Ovo je u skladu sa prirodom prelaska A. cepa, koji ozbiljno pati od inbreed depresije [47]. Ukupni Fis vrijednost izračunata u populacijama luka razmatranih u ovoj studiji (0.054) bila je niža od one koju je prethodno prijavio [45] (0.22) i gotovo identična onoj koju je pronašao [31] (0.08) i [48] (0.00) koji su procijenili genetičku raznolikost u sortama luka iz sjeverozapadne Španije i Nigera. Značajni nivoi heterozigotnosti u ARO populacijama potvrđuju ideju da Apulija predstavlja centar raznolikosti za mnoge hortikulturne vrste [32, 42, 49-jedan].
AMOVA je naglasila da većina molekularnih varijacija u kolekciji genotipiziranoj u ovoj studiji leži unutar populacija. Međutim, značajna genetska diferencijacija među populacijama (FPT vrijednosti) otkrili su pojavu genetske stratifikacije. Zapravo, iako su naši rezultati ukazali na prisustvo genetske uniformnosti u većini ARO populacija, formirajući dobro definiran klaster, populacije ARO7 i ARO12 pokazale su jasno različit genetski profil. Ovaj rezultat bi mogao biti posljedica različitog porijekla sjemena koje su koristila dva farmera od kojih su prikupljene populacije. Štaviše, na osnovu dobijenih rezultata, ARO landrasa se može smatrati jasno različitom na genetskom nivou od TRO i MCO landrasa. U nedavnoj studiji, [29] procijenio je genetsku raznolikost nekoliko talijanskih sorti luka uključujući "Acquaviva", "Tropea" i "Montoro". Iako su autori koristili SNP markere za procjenu genetske raznolikosti šire kolekcije luka, genotipizacija nije bila u stanju da razlikuje “Acquaviva” od “Tropea” i “Montoro” luka. Vjerovatno je ovo odstupanje uzrokovano niskom pronađenom srednjom vrijednosti PIC (0.292), što ukazuje na skromnu opštu informativnost analiziranih lokusa, kako tvrdi [29]. Nadalje, da bi se istražilo prisustvo podstrukture u njihovom talijanskom klasteru, bilo bi bolje analizirati talijanske genotipove odvojeno od ostatka kolekcije. Vjerovatno bi to omogućilo da se vizualizira obrazac genetske raznolikosti povezan s geografskom stratifikacijom ili osobinama pod empirijskom selekcijom.
U zaključku, ova studija predstavlja sveobuhvatan izvještaj o sorti luka koja je povezana s lokalnom kulturnom baštinom i od ekonomskog značaja za poljoprivrednike. Naši rezultati ističu da, uz nekoliko izuzetaka, ARO karakterizira dobro definiran genski fond, koji zaslužuje da bude sačuvan od rizika genetske erozije. Stoga je uspostavljanje reprezentativne kolekcije ovog vrijednog izvora genetske raznolikosti bilo od ključnog značaja. Konačno, genetska i fenotipska karakterizacija ARO bi mogla biti korisna za dobijanje oznaka kvaliteta od Evropske unije.
Materijali i metode
Sakupljanje germplazme, biljni materijal i ekstrakcija DNK
Skup od 13 populacija ARO landrace nabavljen je u okviru projekta regije Apulija (BiodiverSO: https://www.biodiversitapuglia.it/), kroz niz misija sprovedenih u “Acquaviva delle Fonti”, malom apulijskom gradu u provinciji Bari, Italija. Mesta prikupljanja svakog pristupa su mapirana preko Geografskog informacionog sistema (GIS) i prikazana u tabeli 4. Osim toga, dvije populacije iz TRO landrace i jedna populacija iz MCO landrasa uključene su u ovu studiju i korištene kao reference. Sav biljni materijal uzgajan je u istim uslovima životne sredine na eksperimentalnoj farmi “P Martucci” Univerziteta u Bariju (41° 1'22.08″ N, 16°54'25.95″ E), u zaštićenom kavezu kako bi se izbeglo unakrsno oprašivanje među populacije i osiguravanje unutarpopulacijskog oprašivanja pomoću muha puhala (Lucilija Cezar). 16 populacija je okarakterisano po osobinama koje se odnose na veličinu i oblik lukovice i boju kože i mesa (Tabela S1). Osim toga, izvršena je analiza sadržaja čvrste otopine pomoću ručnog refraktometra, a oštrina je mjerena u uzorcima soka od luka dodavanjem 2,4-dinitrofenil hidrazina (0.125% v/v u 2N HCl) i procjenu apsorbancije na 420 nm, kako je izvijestio od [31]. Duncanov test višestrukog opsega i SNK test su sprovedeni da bi se utvrdilo prisustvo značajnih razlika.
Tabela 4. Lista populacija prikupljenih i genotipiziranih u ovoj studiji. Za svaku populaciju izvještavaju se identifikacijski kod, lokalni naziv, GPS koordinate i banka gena koja čuva sjemenke.
| kod | Ime | GPS koordinate | Gene Bank y |
| ARO1 | Cipolla rossa di Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa di Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa di Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa di Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa di Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa di Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa di Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa di Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa di Acquaviva | 40°54'51.372″ N 16°49'3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa di Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa di Acquaviva | 40°52'49.8″ N 16°49'48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa di Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa di Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla rossa lunga di Tropea | - | Di.SSPA |
| TRO2 | Cipolla rossa tonda di Tropea | - | Di.SSPA |
| MKO | Cipolla ramata di Montoro | - | Di.SSPA |
| y Di.SSPA, Odsjek za nauku o zemljištu, biljkama i hrani, Univerzitet u Bariju. |
Materijal lista od 20 genotipova po populaciji je uzorkovan i čuvan na -80 °C do upotrebe. Za vrste bogate polisaharidima, kao A. cepa, Prvi koraci uklanjanja polisaharida su od suštinskog značaja za dobijanje DNK dobrog kvaliteta, stoga su početna ispiranja u STE puferu (0.25 M saharoza, 0.03 M Tris, 0.05 M EDTA) izvedena kako je opisano [52]. Ukupna DNK ekstrahirana je CTAB metodom [53] i konačno je provjerena kvaliteta i koncentracija pomoću Nano Drop 2000 UV-vis spektrofotometra (ThermoScientific, Waltham, MA, USA) i elektroforeze u 0.8% agaroznom gelu.
SSR analiza
16 EST-SSR kombinacija prajmera koje je razvio [54] i prethodno testiran u studijama genetske raznolikosti od strane [43] i [44] i 21 genomski SSR [45-jedan] su pregledani kako bi se ocijenila njihova podobnost (dodatna tabela S4). Genotipizacija je izvedena korištenjem metode ekonomičnog fluorescentnog označavanja u kojoj se M13 rep dodaje svakom prednjem SSR prajmeru [56]. PCR mješavine su pripremljene u 20 gL reakcije koja sadrži: 50 ng ukupne DNK, 0.2 mM mješavine dNTP, 1X pufera za PCR reakciju, 0.8 U DreamTaq DNK polimeraze (Thermo Scientific, Waltham, MA, SAD), 0.16 gM reverznog prajmera , 0.032 gM prednjeg prajmera proširenog sa M13 sekvencom (5′-TGTAAAACGACGGCCAGT-3′), i 0.08 gM univerzalnog prajmera M13 označenog FAM ili NED fluorescentnim bojama (Sigma-Aldrich, St. Louis, MO, SAD). PCR reakcije su izvedene u SimpliAmp (Applied Biosystems, CA, USA) termocikleru sa sljedećim uslovima za većinu parova prajmera: 94 °C 5 min, 40 ciklusa na 94 °C 30 s, 58 °C za 45 s i 72 °C za 45 s i konačno istezanje na 72 °C za 5 min. Što se tiče ACM446 i ACM449, primijenjen je touchdown PCR sa žarenjem od 60 °C do 55 °C tokom 10 ciklusa, 30 ciklusa na 55 °C, nakon čega je uslijedilo konačno produženje od 5 minuta na 72 °C. PCR proizvodi su stavljeni u ploču sa 96 jažica i pomešani sa 14 gL Hi-Di Formamida (Life Technologies, Carlsbad, Kalifornija, SAD) i 0.5 gL GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA). Amplikoni su razdvojeni pomoću mašine za kapilarno sekvencioniranje ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA), gdje su aleli ocijenjeni kao ko-dominantni i dodijeljeni korištenjem GeneMapper softverske verzije 3.7.
Softver GenAlEx 6.5 [57] i Cervus 3.0.7 [58] korišteni su za procjenu broja alela (Na), broja efektivnih alela (Ne), uočene heterozigotnosti (Ho), očekivane heterozigotnosti (He), sadržaja polimorfne informacije (PIC), Shanonovog indeksa informacija (I) i indeksa fiksacije (Fis ) za svaki SSR lokus.
Procjena genetičke raznolikosti
GenAlEx 6.5 procijenio je hijerarhijsku podjelu genetske varijacije između i unutar populacija luka. [57] kroz analizu molekularne varijanse (AMOVA) sa 999 bootstrappingom da bi se testirala značajnost. Štaviše, GenAlEx 6.5 softver je korišten za procjenu raznolikosti unutar svake populacije izračunavanjem prosjeka Ho, He i Fis za sve SSR lokuse.
Struktura stanovništva je zaključena bajesovskim algoritmom za grupisanje zasnovanim na modelu implementiranim u softver STRUCTURE v.2.3.4 [59]. Skup podataka je pokrenut s brojem hipotetičkih klastera (K), u rasponu od 1 do 10, postavljajući deset nezavisnih pokreta za svaku vrijednost K. Za svaku vožnju, u cilju verifikacije konzistentnosti rezultata, 100,000 početnih perioda sagorevanja i 100,000 iteracija Markovskog lanca Monte Carlo (MCMC) izvedeno je prema modelu primjesa i nezavisnim frekvencijama alela među populacijama. Najvjerovatnija vrijednost K određena je primjenom AK metode, opisane od [60], u web baziranom programu STRUCTURE HARVESTER [61]. Pojedinačna populacija je dodijeljena određenom klasteru kada je njen koeficijent pripadnosti (q-vrijednost) bio veći od 0.7, u suprotnom se smatralo da ima pomiješano porijeklo.
Analiza glavnih koordinata obavljena je kako bi se vizualizirali obrasci genetskog odnosa među akcesijama koje je otkrila Neijeva genetička matrica udaljenosti (dodatna tabela S5). Na osnovu frekvencija alela konstruisan je dendrogram genetske udaljenosti implementacijom metode neponderisane grupe parova sa klaster analizom aritmetičkih proseka (UPGMA) u softveru POPTREEW [62]. Bootstrapping je primijenjen za procjenu povjerenja u hijerarhijsko grupiranje, postavljanjem 100 ponovnog uzorkovanja skupa podataka. Konačno, MEGA X softver [63] je korišten kao softver za crtanje stabla.
Dodatni materijali: Sljedeće su dostupne online na http://www.mdpi.com/2223-7747/9/2/260/s1. Tabela S1: Morfološka karakterizacija ARO, MCO i TRO sijalica. Tabela S2: Indeksi heterozigotnosti i fiksacije izračunati za ARO landrase i TRO i MCO landrase. Tablica S3: Parne vrijednosti parametra Fpt. Tabela S4: Lista SSR-ova korištenih u studiji. Tabela S5. Parna populacijska matrica Nei genetske udaljenosti. Slika S1: Linijski grafikon vrijednosti K koje se mijenjaju sa Evannovom Delta K.
Doprinosi autora: CL i LR su osmislili studiju i dizajnirali eksperiment; CL i PI su izvršili analizu molekularnih markera; ARM i VZ su izvršili oglede na terenu; RM, SP, GR i CL su bili uključeni u analizu podataka; RM i CL napisali su rukopis. Svi autori su pročitali i pristali na objavljenu verziju rukopisa.
Finansiranje: Ovaj rad je finansiran od strane regionalnog apulijskog projekta „Biodiverzitet apulijskih vrsta povrća“—Programma di Sviluppo Rurale per la Puglia 2014-2020. Misura 10—Sottomisura 10.2; grant CUP H92C15000270002, Italija.
priznanja: Zahvalnice duguju “Azienda Agricola Iannone Anna” i “Associazione produttori della vera cipolla rossa di Acquaviva” za pružanje biljnih materijala korištenih u eksperimentu.
Sukob interesa: Autori ne objavljuju sukob interesa.
reference
- 1. Stearn, WT Koliko vrsta Alliuma je poznato? Kew Mag. 1992, 9, 180-182. [CrossRef]
- 2. FAOSTAT. FAO Statistical Database. Dostupno na mreži: http://www.fao.org/2017 (pristupljeno 8. januara 2019.).
- 3. Block, E. Hemija bijelog luka i luka. Sci. Am. 1985, 252, 114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Procjena crvenog luka na antioksidativno djelovanje kod pacova. Food Chem. Toxicol. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Moon, J.; Chung, JH; Cha, YJ; Shin, MJ Učinak ekstrakta ljuske luka bogatog kvercetinom na arterijsku trombozu kod pacova. Food Chem. Toxicol. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Efekti ekstrakta luka protiv gojaznosti kod masnih pacova sa dijabetesom Zucker. Nutrijenti 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehman, K.; Chen, S. Začinska biljka Allium cepa: dodatak prehrani za liječenje dijabetes melitusa tipa 2. ishrana 2014, 30, 1128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Inhibicijski efekti luka (Allium cepa L.) ekstrakt na proliferaciju ćelija raka i adipocita putem inhibicije sintaze masnih kiselina. Asian Pac. J. Cancer Prev. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Lien, JC; Tsai, CH; Chung, JG Quercetin inhibira migraciju i invaziju SAS humanih oralnih ćelija raka kroz inhibiciju NF-kappaB i signalnih puteva matriks metaloproteinaze-2/-9. Anticancer Res. 2013, 33, 1941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Češnjak i luk: njihova svojstva prevencije raka. Rak Prev. Res. 2015, 8,181-189. [CrossRef]
- 11. Forte, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Antioksidativna svojstva i svojstva obnavljanja kostiju kvercetin-funkcionaliziranog hidroksiapatita: studija kokulture ćelija osteoblasta-osteoklasta i endotela in vitro. Acta Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Raspodjela jedanaest prekursora okusa, derivata S-Alk(en)il-L-cisteina, u sedam Allium povrća. Food Sci. Technol. Res. 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Hemija organskog sumpora iz roda Allium—implikacije na organsku hemiju sumpora. Angew. Chem. Int. Ed. engl. 1992, 31, 1135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Thomas, B.; Smith, B. Luk – globalna korist za zdravlje. Phytother. Res. 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Enzimski razvoj pirogrožđane kiseline u luku kao mjera ljutine. J. Agric. Food Chem. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CAT; Randle, WM Procjena oštrine u luku. U Provjerene studije za laboratorijsku nastavu; Karcher, SJ, ur.; Udruženje za laboratorijsko obrazovanje za biologiju (ABLE): New York, NY, SAD, 1998; Svezak 19, str. 177-196.
- 17. Hanelt, P. Taksonomija, evolucija i istorija. U Luk i srodni usevi, Vol. I. Botanika, fiziologija i genetika; Rabinowitch, HD, Brewster, JL, Eds.; CRC Press: Boca Raton, FL, SAD, 1990; str. 1-26.
- 18. Rabinowitch, HD; Currah, L. Allium Crop Science: Nedavna dostignuća; CABI Publishing: Wallingford, UK, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Karakterizacija genetskih resursa luka (Allium cepa L.) iz španjolskog sekundarnog centra raznolikosti. Raspon. J. Agric. Res. 2011, 9, 144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Procjena fenola i cistein sulfoksida u lokalnoj germplazmi luka i ljutike iz Italije i Ukrajine. Genet. Resour. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Morfološki, nutritivni i hemijski opis 'vatikiotiko', lokalne sorte luka iz Grčke. Food Chem. 2015,182, 156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Biohemijska, antioksidativna svojstva i antimikrobna aktivnost različitih sorti luka na području Mediterana. J. Food Meas. Karakter. 2019,13, 1232-1241. [CrossRef]
- 23. Yoo, KS; Pike, L.; Crosby, K.; Jones, R.; Leskovar, D. Razlike u oštrini luka zbog sorti, okruženja rasta i veličine lukovica. Sci. Hortic. 2006,110, 144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; George, E.; Kroh, LW; Rohn, S. Distribucija kvercetin-3, 4′-O-diglukozida, kvercetin-4′-O-monoglukozida i kvercetina u različitim dijelovima lukovice luka (Allium cepa L.) pod utjecajem genotipa. Food Chem. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchionna, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Utjecaj vremena presađivanja i gustine biljaka na prinos, kvalitet i sadržaj antioksidansa crnog luka (Allium cepa L.) u južnoj Italiji. Sci. Hortic. 2014,166, 111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Povećanje dodane vrijednosti luka kao izvora antioksidativnih flavonoida: Kritički pregled. Krit. Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Utjecaj metode uzgoja i selekcije sorte na rastvorljive ugljikohidrate i opor principe u luku (Allium cepa L.). J. Agric. Food Chem. 2018, 66, 12827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identifikacija i kvantifikacija flavonoida iz dvije južnotalijanske sorte allium cepa L., Tropea (crveni luk) i Montoro (luk bakra), i njihov kapacitet zaštite ljudskih eritrocita od oksidativnog stresa. J. Agric. Food Chem. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. Genotipizacija visoke propusnosti u luku otkriva strukturu genetičke raznolikosti i informativne SNP-ove korisne za molekularni uzgoj. Mol. Breed. 2019, 39, 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Genetička varijacija italijanskog paradajza sa dugim rokom trajanja (Solanum lycopersicum L.) prikupljanje korištenjem SSR i morfoloških osobina ploda. Genet. Resour. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perović, D.; Silvar, C. Istraživanje genetske raznolikosti i osobina kvaliteta u kolekciji luka (Allium cepa L.) landrase iz sjeverozapadne Španjolske. Genetika 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. Genetička, bio-agronomska i nutritivna karakterizacija kelja (Brassica oleracea L. var. acephala) raznolikost u Apuliji, južna Italija. raznovrsnost 2018,10, 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. Genetička analiza rezistencije na Orobanche crenata (Forsk.) u grašku (Pisum sativum L.) niskostrigolaktonska linija. J. Plant Pathol. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Mapiranje lokusa kvantitativnih svojstava za vrijeme spajanja luka u grozdovima (Allium fistulosum L.). Eufitika 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Identifikacija genskih SSR-a i izgradnja mape veza zasnovane na SSR-u u Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Mote, SR; Gopal, J. Evaluacija sortnog identiteta luka korištenjem SSR markera. Seed Sci. Technol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. Izbor i validacija seta markera za diferencijaciju sorti luka iz Češke. Češki J. Genet. Plant Breed. 2015, 51, 62-67. [CrossRef]
- 38. Di Rienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Očuvanje i karakterizacija biodiverziteta apulijske germplazme masline. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. Procjena genetske raznolikosti španjolskog jezika allium cepa landrase za uzgoj luka pomoću mikrosatelitskih markera. Sci. Hortic. 2014,170, 24-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Procjena genetske raznolikosti luka (allium cepa L.) landrase iz sjeverozapadne Španjolske i poređenje s europskom varijabilnosti. NZJ Crop Hortic. 2016, 44, 103-120. [CrossRef]
- 41. De Giovanni, C.; Pavan, S.; Taranto, F.; Di Rienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Genetička varijacija globalne kolekcije germplazme slanutka (Cicer arietinum L.) uključujući i italijanske članove koji su u opasnosti od genetske erozije. Physiol. Mol. Biol. Biljke 2017, 23, 197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Genetička raznolikost u brokuli rabe (Brassica rapa L. subsp. sylvestris (L.) Janč.) iz južne Italije. Sci. Hortic. 2019, 253, 140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Pojedinačni nukleotidni polimorfizmi, indeli i jednostavni ponavljanja sekvenci za identifikaciju sorte luka. J. Am. Soc. Hortic. Sci. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Analiza genetičke raznovrsnosti i razvoj markera polimorfizma jednog nukleotida u kultivisanom luku lukovice na osnovu ekspresirane sekvence tag-jednostavne sekvence ponavljanja markera. J. Am. Soc. Hortic. Sci. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Razvoj robusnih genomskih markera ponavljanja jednostavne sekvence za procjenu genetičke raznolikosti unutar i među lukovicama luka (Allium cepa L.) populacije. Mol. Breed. 2012, 30, 1401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Mikrosatelitski markeri kod bijelog jelena. J. Hered. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. Iranski luk (Allium cepa L.) reakcije sorti na depresiju kod inbreedinga. World Appl. Sci. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Genetička raznolikost nigerskog luka (Allium cepa L.) procijenjen jednostavnim markerima ponavljanja sekvence (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Taranto, F.; D'Agostino, N.; Schiavulli, A.; et al. Izrazita genetska grupa u uzgojenom slanutku, što je otkriveno otkrivanjem markera u cijelom genomu i genotipizacijom. Plant Genome 2017, 2017,10. [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotipizacija-sekvenciranjem dinje (Cucumis melo L.) zbirka germplazme iz sekundarnog centra raznolikosti naglašava obrasce genetske varijacije i genomske karakteristike različitih genskih fondova. BMC Genom. 2017, 18, 59. [CrossRef]
- 51. Di Rienzo, V.; Sion, S.; Taranto, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Bouchefa, S.; Tamenđari, A.; Pasqualone, A.; et al. Genetski tok među populacijom maslina unutar mediteranskog bazena. Peer J. 2018, 6. [CrossRef]
- 52. Shepherd, LD; McLay, TG Dva protokola mikro-razmjera za izolaciju DNK iz biljnog tkiva bogatog polisaharidima. J. Plant Res. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Izolacija biljne DNK iz svježeg tkiva. fokus 1990,12, 13-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Sudoper, KC; Jenderek, M.; et al. Jedinstveni set od 11,008 oznaka sekvence izražene u luku otkriva ekspresnu sekvencu i genomske razlike između redova monosupčanika i poala. Biljna ćelija 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Song, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Razvoj markera za testiranje genetske čistoće luka koristeći SSR Finder. Korean J. Breed. Sci. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Ekonomska metoda za fluorescentno obilježavanje PCR fragmenata. Nat. Biotechnol. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Genetička analiza u Excelu. Populacioni genetski softver za nastavu i istraživanje: ažuriranje. Bioinformatika 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Taper, ML; Marshall, TC Revizija načina na koji kompjuterski program CERVUS prilagođava greške genotipizacije povećava uspjeh u određivanju očinstva. Mol. Ecol. 2007,16, 1099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Mapiranje asocijacija u strukturiranim populacijama. Am. J. Hum. Genet. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Detekcija broja klastera pojedinaca pomoću softvera STRUKTURA: simulacijska studija. Mol. Ecol. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. STRUKTURA HARVESTER: Web stranica i program za vizualizaciju izlaza STRUKTURA i implementaciju Evanno metode. Conserv. Genet. Resour. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: Web verzija POPTREE za konstruisanje stabala populacije iz podataka o frekvenciji alela i izračunavanje nekih drugih veličina. Mol. Biol. Evol. 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Analiza molekularne evolucione genetike na računarskim platformama. Mol. Biol. Evol. 2018, 35, 1547-1549. [CrossRef]